¡Buenas amigos!
Hoy intentaré relacionar lo aprendido en las entradas de Radiación Beta y Radiación Alfa con el estudio de la antigüedad de rocas, fósiles...
Lo primero de todo es recordar que en la Naturaleza existen 4 fuerzas fundamentales: Gravitación, Electromagnetismo, Nuclear Fuerte y Nuclear Débil. En esta tabla se recogen los datos más relevantes de estas fuerzas:
Los estudios sobre Gravitación se los debemos en primera instancia a Newton (Ley de la Gravitación Universal), y dos siglos después a Einstein (Teoría General de la Relatividad). Es una fuerza universal, que disminuye con la distancia, presente entre todas las partículas con masa, de carácter atractivo. Su partícula correspondiente, aún no confirmada experimentalmente, es el Gravitón. Es la fuerza más "débil", ya que un simple imán atrayendo un clip de metal supera la fuerza que la Tierra ejerce sobre ese clip, por ejemplo.
La unificación entre electricidad y magnetismo se lo debemos en gran medida al físico inglés Maxwell. Es una fuerza asociada a la carga, cuya partícula es el fotón (sin masa en reposo y por tanto su velocidad es la de la luz). Tiene un alcance universal, disminuye con la distancia, y puede ser tanto atractiva como repulsiva. Es la segunda fuerza más intensa después de la Nuclear Fuerte.
Ya en el siglo XX, gracias al estudio del núcleo atómico, consiguió estudiarse la interacción fuerte y la débil. La fuerte es la encargada de mantener a los protones y neutrones fijos en el núcleo atómico, aunque su alcance es ínfimo. La partícula correspondiente es el gluón (en inglés glue es pegamento), y es la más intensa de las 4.
Finalmente, la Fuerza Débil (sigue siendo muy intensa, que su nombre no nos engañe...) llamada así porque es menos intensa que la Fuerte, es la encargada del decaimiento beta tan imprescindible en la fusión nuclear de las estrellas. Cambia el sabor de los quarks constituyentes de los nucleones, y su partícula asociada son los bosones W y Z. Tiene un alcance aún menor que la anterior, debido a que los bosones W y Z tienen una vida muy corta, menor que la de los gluones.
La perfecta armonía de estas cuatro fuerzas hace posible la existencia del universo tal y como lo conocemos.
¿Alguna vez os habéis preguntado por qué no se repelen los protones de los núcleos atómicos?
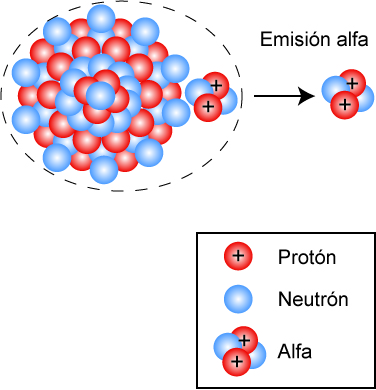
La respuesta es que la fuerza nuclear fuerte actúa de enlace entre ellos, superando a la fuerza electrostática de repulsión. A medida que un átomo es más y más grande, y dado que la fuerza electromagnética tiene alcance infinito mientras que la nuclear fuerte es de corto alcance, el núcleo tiende a ser más y más inestable. Llega un momento en que la fuerza de repulsión supera con creces a la nuclear fuerte, y entonces el átomo se divide en otros dos más ligeros liberándose gran cantidad de energía y partículas alfa. Es el proceso de fisión nuclear.
Por otra parte, la interacción débil es la responsable de la radiación beta (tanto positiva como negativa). Tal y como vimos en la entrada correspondiente, que puedes visitar aquí, los neutrones y los protones están transformándose continuamente (los protones se transforman en neutrones y los neutrones en protones, quedando el átomo tal cual). El problema está en los isótopos con demasiados neutrones, donde este proceso no ocurre del mismo modo. En estos casos, hay una cierta probabilidad de que un neutrón decaiga en un protón, aumentando en uno el número atómico del elemento, sin que otro protón decaiga en neutrón. Cuanto más pesado sea el isótopo, más probable es este proceso.
Cuando ocurre esto, el bosón W-, encargado de cambiar el sabor del quark correspondiente para la transformación del protón en neutrón, se desintegra. En su desintegración se produce un electrón (conservando la carga) y un antineutrino (para conservar parte de la energía en energía cinética). Puede ocurrir que halla demasiados pocos neutrones y que un protón decaiga en un neutrón. En este caso se liberaría un bosón W+, que decae en un positrón (antipartícula correspondiente al electrón) y un neutrino.
 |
| En neutrón (n) decae en un protón (p), un electrón (e) y un antineutrino (v) |
¿Qué tiene que ver todo esto con la datación en rocas y seres vivos?
En las rocas, como en los seres vivos, hay isótopos radiactivos que nos pueden ayudar a datar la edad de una roca o un fósil. Hay tres mecanismos dependiendo de los isótopos implicados en el proceso de datación:
Ocurre cuando un elemento aumenta el número de protones de su núcleo. Un ejemplo es el Carbono 14, que decae en Nitrógeno 14 (con un protón más y un neutrón menos). En el proceso se liberan electrones del núcleo en forma de radiación y también antineutrinos. El tiempo que tarda la mitad de una muestra en desintegrarse son 5570 años, tiempo que se llama vida media. Estudiando la relación entre átomos de carbono y de nitrógeno podemos saber la edad del fósil. Es útil en restos de seres vivos. Los seres vivos intercambian Carbono 14 con el medio ambiente hasta que mueren. A partir de ese momento éste se va desintegrando en Nitrógeno 14, proceso que utilizamos para datarlo.
Un elemento disminuye su número atómico. El Potasio 40 decae en Argón 40, ya que uno de sus protones decae en un neutrón. Se libera en el proceso un positrón y un neutrino. Es el método más usado, y la desintegración de la mitad de una muestra tarda 1.300 millones de años.
Es usada en átomos más grandes, como el Uranio, y es el método más preciso. Debido al corto alcance de la fuerza Fuerte, el átomo de Uranio 235 se rompe y se forma el átomo de Plomo 207, liberándose en el proceso partículas alfa (núcleos de helio) y energía, mucha energía. Por esta razón son frecuentes los depósitos de helio cerca de las minas de uranio.
Y hasta aquí la entrada de hoy. Si os ha gustado, dejad un comentario y compartid a quienes creáis que les pueda gustar. Un saludo y hasta la próxima.




.jpg)